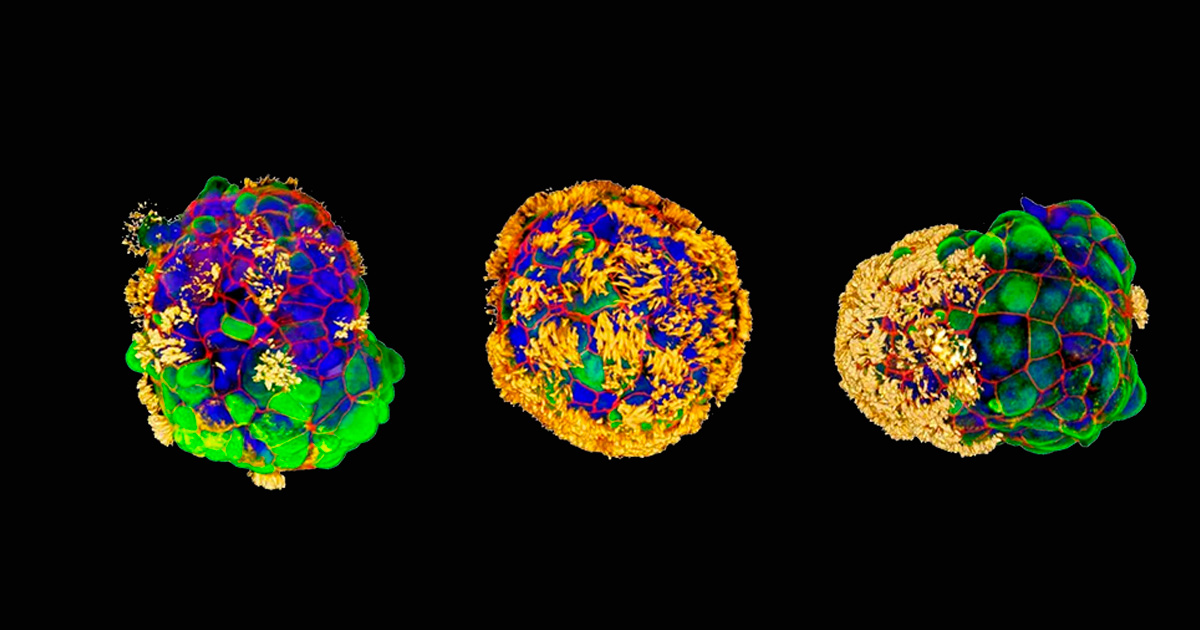
Un equipo de investigadores ha conseguido crear robots biológicos microscópicos a partir de células cosechadas de tráqueas humanas.
Bautizados como antrobots, estos minirrobots multicelulares son capaces de autoensamblarse, de moverse a través de diferentes superficies y de ayudar a curar lesiones en neuronas cultivadas en el laboratorio. Podrían convertirse en una esperanza para tratar enfermedades hoy difíciles de tratar o incurables, como las lesiones medulares, ciertos cánceres y los ictus e infartos.
Los robots multicelulares, esto es, que se componen de más de una célula, pueden alcanzar diversos tamaños, desde el calibre de un pelo humano hasta el diámetro de la punta de un lápiz afilado. El sensacional descubrimiento constituye un punto de partida para el diseño de nuevas terapias médicas, ya que podrían utilizarse biobots derivados de pacientes como prometedoras herramientas terapéuticas para la regeneración, la curación y el tratamiento de enfermedades rebeldes.
Los pormenores de este avance científico aparecen detallados en un artículo publicado en la revista Advanced Science por investigadores de la Universidad Tufts, el Instituto Wyss de la Universidad de Harvard y el Instituto de Tecnología de Nueva Jersey (EE. UU.).
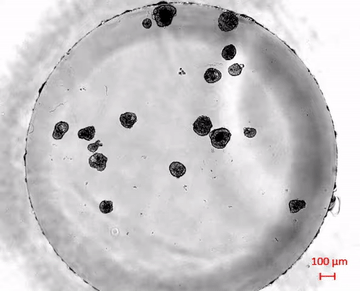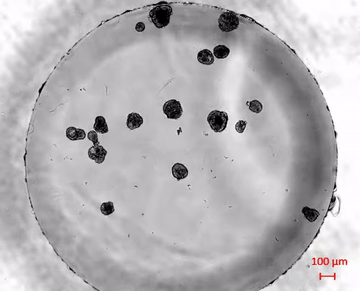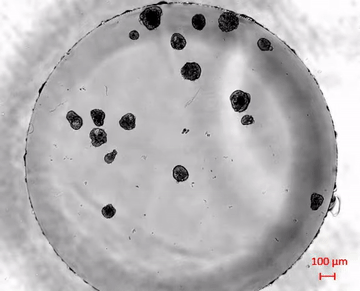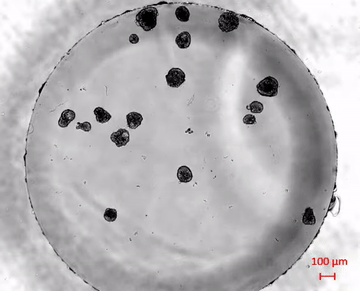
La evolución de los robots biológicos
Los antrobots nacen de investigaciones anteriores llevadas a cabo en los laboratorios de Michael Levin, biólogo de la Facultad de Artes y Ciencias en la Universidad Tufts, y Josh Bongard, de la Universidad de Vermont. En 2021, estos expertos presentaron a la prensa unos robots biológicos multicelulares creados a partir de células de embriones de rana que llamaron xenobots.2, una versión mejorada de unos robots biológicos en los que llevaban tiempo trabajando y que eran capaces de autoensamblarse, no necesitaban células musculares para moverse e incluso mostraban capacidad de memoria grabable.
Los xenobots.2 eran capaces de navegar por pasadizos, recolectar material, registrar información, autorrepararse e incluso replicarse durante algunos ciclos por sí solos. En ese momento, Levin y Bongard no sabían si estas capacidades surgían de las propias células embrionarias del anfibio o si, por el contrario, estos biobots podrían construirse a partir de células de otras especies.
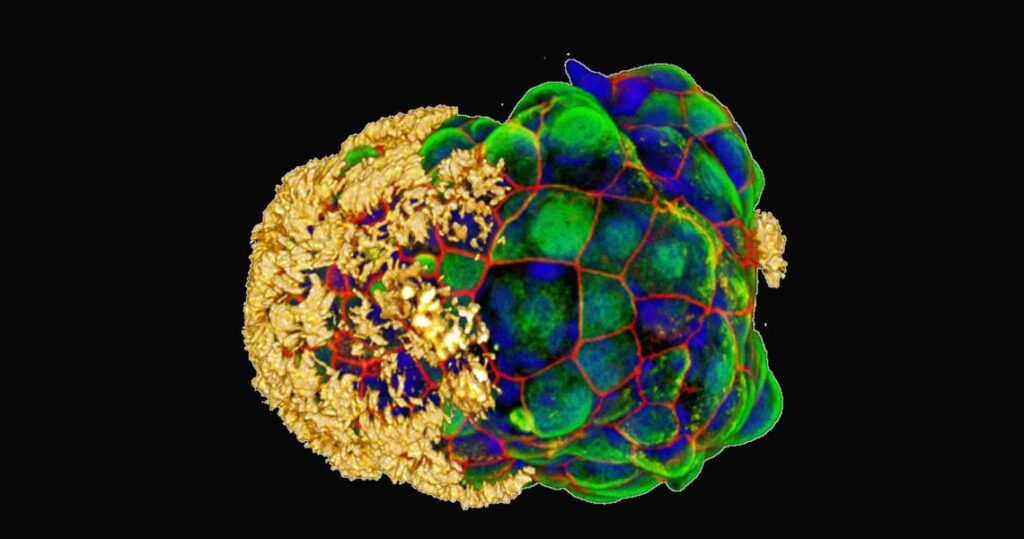
En el nuevo proyecto, Levin, junto con la estudiante de doctorado Gizem Gumuskaya, descubrió que, de hecho, se pueden crear robots a partir de células humanas adultas sin necesidad de llevar a cabo ninguna modificación genética y que exhiben algunas capacidades que van más allá de las observadas en los xenobots.
De hecho, los antrobots han proporcionado pistas para responder a una pregunta que se planteó el equipo de Levin en el laboratorio: ¿cuáles son las reglas que rigen el modo en que las células se ensamblan y trabajan juntas en tejidos y órganos? Es más, ¿es posible sacar a las células de su contexto natural y que se recombinen en diferentes planes corporales para llevar a cabo otras funciones programadas?
Para ahondar en esta cuestión, Levin y Gumuskaya dieron a las células humanas, después de décadas de llevar una apacible vida en la tráquea, la oportunidad de reiniciarse y encontrar formas de crear nuevas estructuras y tareas. «Queríamos investigar qué pueden hacer las células además de crear características predeterminadas en el cuerpo —comenta Gumuskaya. Y añade—: Al reprogramar las interacciones entre células, se pueden crear nuevas estructuras multicelulares, de forma análoga al modo en que la piedra y el ladrillo se pueden organizar en diferentes elementos estructurales como paredes, arcos o columnas».
Los investigadores descubrieron que las células no solo podían crear nuevas formas multicelulares, sino que también eran capaces de moverse de diferentes maneras sobre una pradera de neuronas humanas cultivadas en el laboratorio, dentro de los límites de una placa de Petri. Por si esto fuera poco, sus antrobots tenían la virtud de estimular el crecimiento de las células nerviosas allí donde los investigadores habían creado un hueco al raspar una pequeña área en el mantel de neuronas.
De los antrobots a los superbots
Levin y su equipo aún no han conseguido dilucidar cómo los antrobots estimulan el crecimiento de las neuronas, aunque sí han visto que estas células nerviosas se multiplican cuando actúan a la vez un conjunto de antrobots. A este equipo lo han bautizado como superbot.
«Los conjuntos celulares que construimos en el laboratorio pueden tener capacidades que van más allá de lo que hacen en el cuerpo —explica Levin en una nota de prensa del Instituto de Tecnología de Nueva Jersey. Y continúa—: Resulta fascinante y completamente inesperado comprobar que las células traqueales de pacientes normales, sin modificar su ADN, puedan moverse por sí solas y estimular el crecimiento neuronal en una región dañada. Ahora estamos analizando cómo funciona el mecanismo de reparación y preguntándonos qué más pueden hacer estas construcciones».
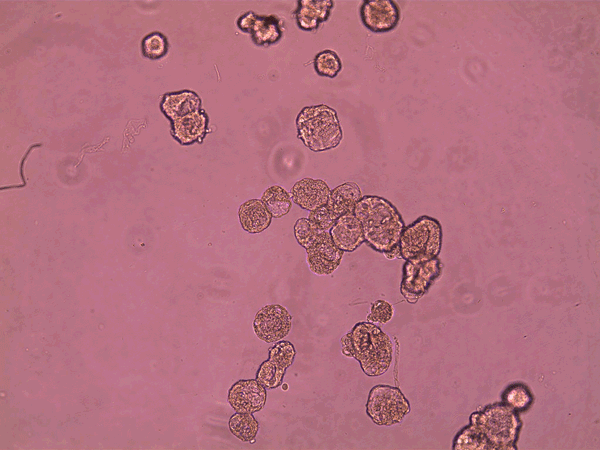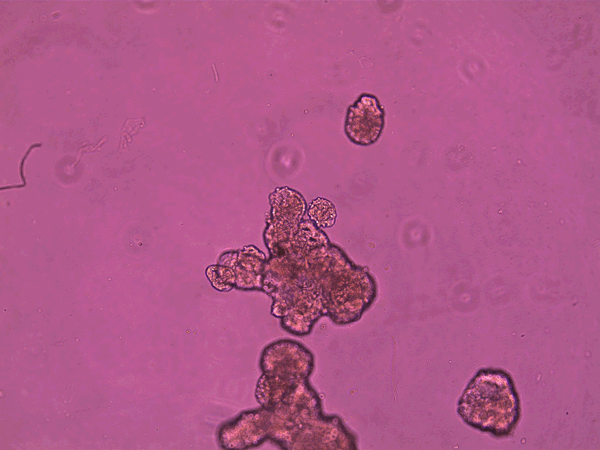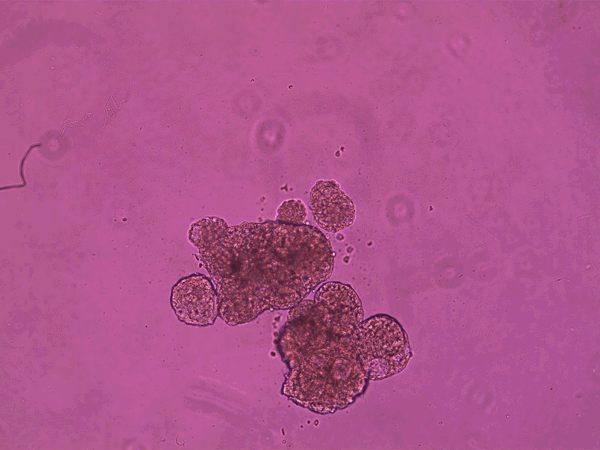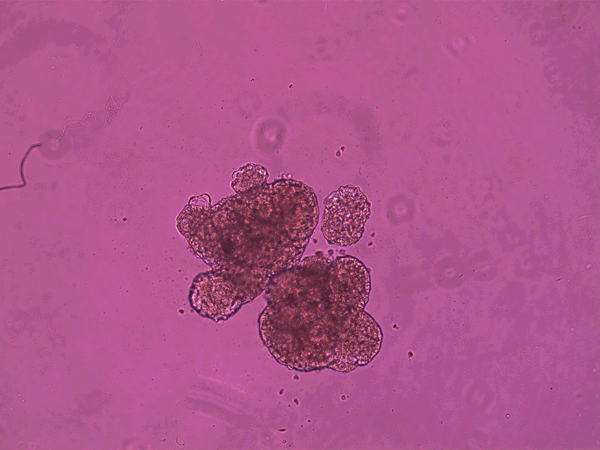
Los antrobots hacen su trabajo, se degradan y son reabsorbidos por el organismo
Las ventajas de utilizar células humanas incluyen la capacidad de construir robots a partir de las propias células del paciente para llevar a cabo trabajos terapéuticos sin el riesgo de desencadenar una respuesta inmunológica o tener que echar mano de agentes inmunosupresores. Otro atributo positivo de los antrobots es que después de realizar su cometido, que puede alargarse desde unos días a unas semanas, se descomponen y los restos son reabsorbidos por el organismo de manera limpia y natural.
Por otro lado, los antrobots son bastante seguros. En palabras de Levin, solo pueden sobrevivir en condiciones muy específicas y no hay riesgo de exposición o propagación involuntaria más allá de las puertas del laboratorio. Asimismo, no se reproducen y no sufren ediciones, adiciones o eliminaciones genéticas, por lo que no hay riesgo de que evolucionen más allá de las salvaguardas existentes.
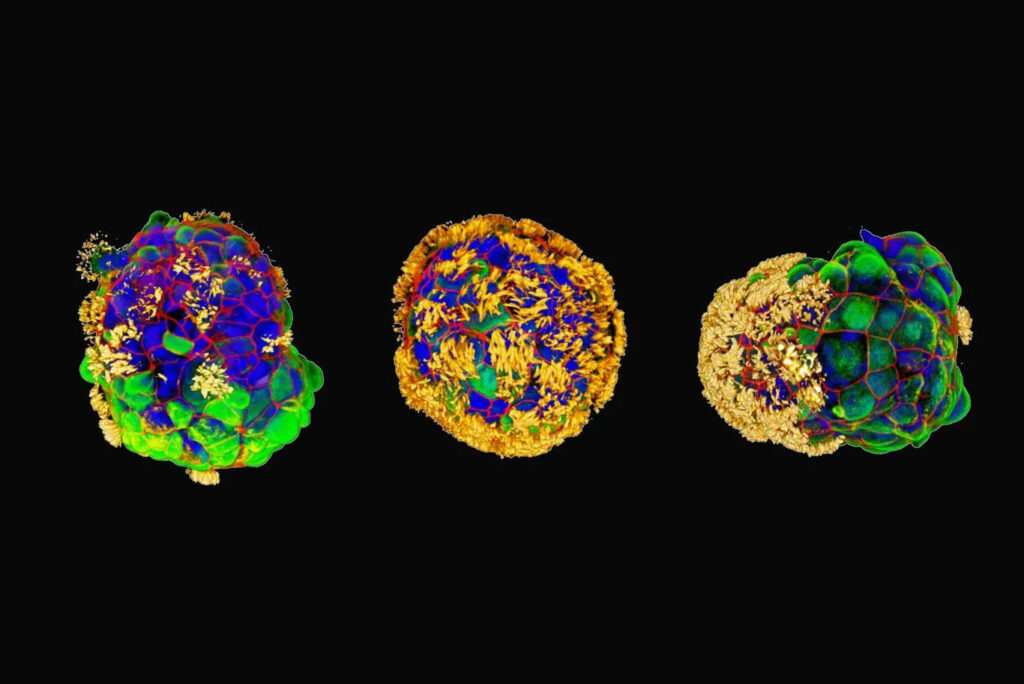
Así se fabrican los robots biológicos
Pero ¿cómo nacen los antrobots? Cada uno de ellos comienza como una célula única, que procede de un donante humano. En concreto, son células que provienen de la tráquea y que están cubiertas por proyecciones parecidas a pelos llamadas cilios, que, a modo de remos, se mueven hacia adelante y hacia atrás. Cada célula traqueal cuenta con unos doscientos cilios, con cuyo movimiento desplazan la capa de moco que cubre la superficie de la tráquea y cualquier partícula que haya pegada sobre ella hacia la laringe. Por tanto, se encargan de limpiar los pulmones de partículas que entran durante la respiración.
Estudios anteriores realizados por otros autores habían demostrado que cuando estas células cepillo se cultivan en el laboratorio, forman espontáneamente pequeñas esferas multicelulares llamadas organoides. Sabido esto, Levin y Gumuskaya crearon unas condiciones de crecimiento que propiciaron que los cilios miraran hacia afuera en los organoides. A los pocos días, las pelotas celulares empezaron a moverse como critters, impulsados por los cilios que actuaban como remos y, lo no menos importante, con diferentes formas y tipos de movimiento.
En este sentido, Levin opina que, si se pudieran sumar otras características a los antrobots, por ejemplo, las aportadas por células distintas a las traqueales, se podrían reconfigurar para que respondieran a su entorno, así como para que viajaran y realizaran funciones específicas en el organismo o ayudasen a construir tejidos diseñados en el laboratorio.
Su tamaño va desde el grosor de un cabello humano hasta el de la punta de un lápiz afilado
El equipo de Levin, con la asistencia de Simon Garnier, del Instituto de Tecnología de Nueva Jersey, caracterizó los diferentes tipos de antrobots que emergieron en el laboratorio. Observaron que podían clasificarse en unas pocas categorías discretas de forma y movimiento, cuyo tamaño oscilaba entre los 30 y los 500 micrómetros (desde el grosor de un cabello humano hasta el de la punta de un lápiz afilado). De este modo, los antrobots llenaban un nicho importante entre los nanorrobots y los dispositivos de ingeniería de mayor tamaño.
Algunos eran esféricos y estaban completamente cubiertos de cilios, y otros eran irregulares o tenían forma de balón de fútbol con una cobertura de cilios más irregular, o simplemente estaban cubiertos de cilios solo en un lado. Podían viajar en línea recta, avanzar en círculos cerrados, combinar estos dos movimientos o simplemente se quedaban de brazos cruzados y serpenteaban. El abanico de posibles movimientos resultó ser maravilloso.
Por lo general, los antrobots sobrevivían entre 45 y 60 días en condiciones de laboratorio antes de biodegradarse de forma natural. «Los antrobots se autoensamblan en las placas de laboratorio —precisa Gumuskaya, que, por cierto, es la creadora de estos biorrobots—. A diferencia de los xenobots, no necesitamos pinzas ni bisturís para darles forma, y podemos utilizar células adultas, incluso células de pacientes ancianos, en lugar de células embrionarias. Es totalmente escalable: podemos producir enjambres de estos robots en paralelo, lo cual es un buen comienzo para desarrollar una herramienta terapéutica».
Tanto Gumuskaya como Levin están convencidos de que sus robots multicelulares podrían jugar un papel nada desdeñable en medicina. Para cerciorarse de sus posibles usos terapéuticos, se pusieron manos a la obra y diseñaron un antrobot capaz de curar heridas. El paso siguiente fue cultivar una capa bidimensional de neuronas humanas y, simplemente rascando su superficie con una fina varilla de metal, crearon una herida abierta, o sea, libre de células nerviosas.
Para garantizar que la brecha estuviera expuesta a una densa concentración de antrobots, Levin y Gumuskaya echaron mano de sus superbots, que surgen de manera espontánea cuando un grupo de antrobots está confinado en un espacio reducido. Pues bien, los superbots crearon un puente de neuronas tan grueso como el de la capa bidimensional original. Las neuronas no crecieron en la herida donde no había antrobots. Al menos en el mundo 2D simplificado de la placa de laboratorio, los conjuntos de antrobot fomentaron la curación eficiente del tejido neural vivo.
Según los investigadores, un mayor desarrollo de los robots podría conducir a otras aplicaciones, como es la eliminación de la acumulación de placa en las arterias de pacientes con aterosclerosis, la reparación de daños en la médula espinal o los nervios de la retina, el reconocimiento de bacterias o células cancerosas o la administración de medicamentos a tejidos específicos. En teoría, los antrobots podrían ayudar a curar los tejidos y al mismo tiempo administrar medicamentos prorregenerativos.
Aprovechar las reglas intrínsecamente flexibles del ensamblaje celular ayuda a los científicos a construir los robots biológicos, pero también puede servir para comprender cómo se ensamblan los planes corporales naturales, cómo el genoma y el entorno colaboran para crear tejidos, órganos y extremidades, y cómo estos, cuando sufren daños, pueden repararse con tratamientos regenerativos.
Si los antrobots serán capaces de cumplir estos sueños biomédicos, el tiempo lo dirá.
TAMBIÉN TE PUEDE INTERESAR: