Científicos del Instituto Tecnológico de Massachusetts (MIT), en Estados Unidos, han desarrollado un sistema artificial capaz de detener una hemorragia interna, lo que podrá ayudar a que más personas logren sobrevivir el tiempo suficiente como para llegar a un hospital después de sufrir una grave lesión traumática. Dos componentes se unen justo en la herida para formar un coágulo, esto es, sin hacerlo en partes sanas del cuerpo, donde el tapón podría ser altamente peligroso.
Los eventos traumáticos, como los accidentes de tráfico, los deportivos y los laborales, y las lesiones en el campo de batalla pueden causar hemorragias internas, esto es, una pérdida de sangre en el sistema vascular dentro del organismo; puede ocurrir en la cavidad abdominal, en la cavidad torácica, en el aparato digestivo o en los tejidos que rodean los grandes huesos, caso del fémur y la pelvis, cuando se rompen o desgarran. Se trata de una emergencia médica y el grado de gravedad depende de la velocidad y la ubicación del sangrado; y si la persona afectada no llega a tiempo a urgencias, el desenlace puede ser fatal. Encontrar formas de frenar el sangrado puede extender dicha ventana, lo que sin duda alguna podría salvar numerosas vidas. Sin ir más lejos, solo en España, en 2021, casi 36.000 personas padecieron una conmoción y hemorragias internas asociadas a lesiones ocurridas en el lugar de trabajo; de ellas, 89 fallecieron, según el Ministerio de Trabajo y Economía Social. Y los accidentes automovilísticos causan más de 2,5 millones de muertes anuales en todo el mundo.
Nanopartículas y polímeros en acción
Ahora, un equipo de bioingenieros del MIT ha desarrollado un sistema sintético que puede ser inyectado por los propios técnicos de emergencias sanitarias y que detiene la hemorragia interna en el lugar preciso de la lesión. Lo logra gracias a la participación de unas nanopartículas y unos polímeros que impulsan la formación de coágulos sanguíneos naturales.
No hay que olvidar que nuestro organismo posee los mecanismos biológicos para sellar una hemorragia y mantener el flujo del líquido rojo. En concreto, el llamado sistema hemostático es el encargado de evitar la pérdida de sangre en heridas a través de precisas interacciones entre ciertos componentes que se concentran en las paredes de los vasos sanguíneos, las plaquetas circulantes y determinadas proteínas plasmáticas. Los primeros en acudir a la zona de la rotura vascular son las citadas plaquetas, fragmentos de células muy grandes de la médula ósea, los llamados megacariocitos, que se unen para formar un trombo capaz de sellar la hemorragia (hemostasia primaria). Posteriormente ocurre una serie de reacciones del sistema plasmático de coagulación que culminan en la producción de gran cantidad de trombina, una enzima que contribuye a que un factor de coagulación llamado fibrinógeno se convierta en fibrina. Esta proteína posee la capacidad de formar redes tridimensionales que actúan a modo de pegamento o hilo que mantiene unidas a las plaquetas (hemostasia primaria).
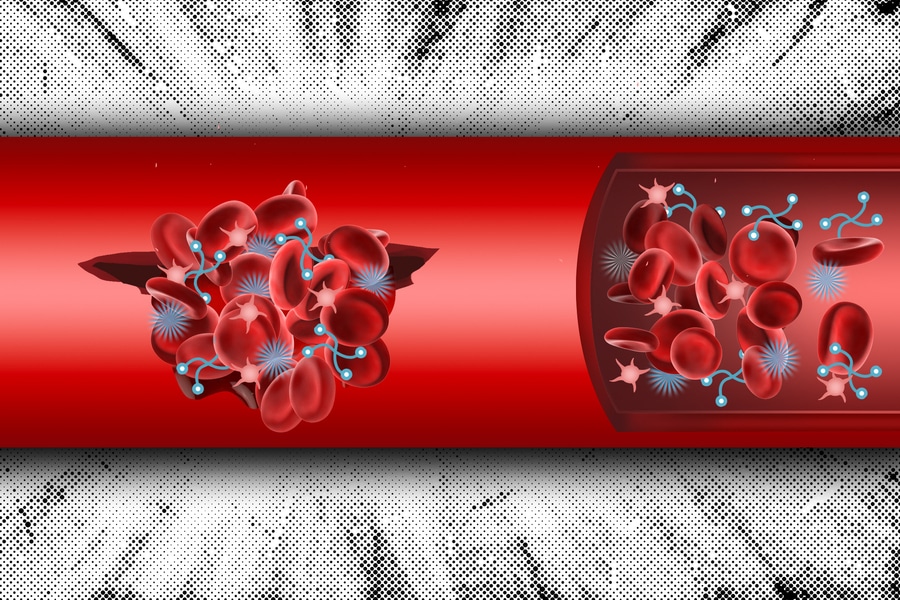
Ingenieros del MIT han diseñado nanopartículas sintéticas que se pueden inyectar en el cuerpo y ayudar a formar coágulos de sangre en los sitios de lesiones internas. Foto Christine Daniloff_MIT
Cómo reclutar plaquetas
Ahora bien, cuando la lesión vascular es importante, el sistema de hemostasia se ve literalmente desbordado y la vida del herido puede verse comprometida. Así es, si los pacientes pierden mucha sangre, no tienen suficientes plaquetas ni fibrinógeno para formar coágulos. Para más inri, ciertas hemorragias internas en órganos vitales, como el hígado, son difíciles de detectar. En estos casos, se requiere de intervención médica. A diferencia de los sistemas hemostáticos desarrollados hasta la fecha, la nueva tecnología del MIT copia la labor de los actores biológicos que participan en la reparación vascular: unas nanopartículas reclutan a las plaquetas circundantes y un polímero imita al fibrinógeno. Las nanopartículas están hechas de un material biocompatible llamado PEG-PLGA y cuentan con un péptido —cadena de aminoácidos— que las ayuda a unirse a las plaquetas activadas. Esto significa que se acumulan donde hay mayor concentración plaquetaria, como ocurre en una herida, y trabajan para atraer más plaquetas al lugar de la hemorragia interna. El tamaño de dichas nanopartículas es de 140 a 220 nanómetros —un nanómetro equivale a una milmillonésima parte de un metro—, lo que evita que se acumulen en órganos como los pulmones, donde los coágulos pueden ser muy peligrosos.
Unos coágulos más fuertes
El ingenio coagulante ha sido probado con éxito en ratones. «Nos llamó poderosamente la atención el nivel de recuperación de las lesiones graves que padecían los animales de laboratorio. La aplicación de dos sistemas complementarios de manera secuencial permite obtener un coágulo mucho más sólido», dice Paula Hammond, una de las autoras del trabajo y jefa del Departamento de Ingeniería Química del MIT. En este particular insiste su colega, el profesor de Ingeniería Química Bradley Olsen: «La idea de usar dos componentes permite la gelación [formación de un gel a partir de un sistema con polímeros] selectiva del sistema hemostático a medida que aumenta la concentración de aquellos en la herida, lo que imita el efecto final de la cascada de sucesos que ocurren durante la coagulación natural».
Es importante destacar que el equipo del MIT también creó lo que han venido a denominar un sistema de reticulación, que cuenta con un grupo químico pegado a las nanopartículas que se une a una etiqueta pegada al polímero que imita al fibrinógeno. Esto ayuda a que los dos componentes del sistema de coagulación sintética se encuentren en el lugar de la rotura vascular y la taponen de manera más eficiente, según Celestine Hong, autora principal del estudio. «Cuando ambos componentes están en alta concentración, se obtiene una mayor reticulación y comienzan a formar ese pegamento necesario para el proceso de coagulación —explica Hong. Y precisa—: Hasta ahora, los científicos que trabajan en este campo han tratado de recuperar los efectos terapéuticos de las plaquetas o de la función del fibrinógeno. Sin embargo, lo que nosotros estamos tratando de conseguir en este proyecto es recrear la forma en que uno y otro interactúan entre sí».
En el futuro, permitirá localizar rápido el lugar de la hemorragia interna
En los experimentos animales, los científicos del MIT han descubierto que después de ser inyectado en el cuerpo, el sistema de dos componentes es muy eficaz para detener el sangrado y funciona aproximadamente el doble de bien que la nanopartícula por sí sola. Otra ventaja importante de los coágulos creados de esta manera es que no se degradan tan rápido como los naturales. Cuando los pacientes pierden mucha sangre, generalmente se les administra una solución salina por vía intravenosa para mantener alta la presión arterial, pero este suero fisiológico también diluye las plaquetas y el fibrinógeno que circulan por el torrente sanguíneo, lo que genera coágulos más débiles y una degradación de estos más rápida. Sin embargo, los coágulos artificiales no son tan susceptibles a este tipo de degradación, según los investigadores.
Satisfechos con los resultados, los científicos ya trabajan en probar el sistema coagulante en animales más grandes y, a largo plazo, tienen en mente explorar la posibilidad de utilizar dispositivos de imagen portátiles para visualizar las nanopartículas inyectadas después de ser inyectadas en el organismo. Esto podría ayudar a los médicos o al personal de emergencias médicas a determinar rápidamente el sitio de la hemorragia interna, lo que actualmente solo se puede hacer en un hospital con resonancia magnética, ultrasonido o cirugía.
Artículo publicado por Enrique Coperías
TAMBIÉN TE PUEDE INTERESAR:
- Llegan los vendajes ‘inteligentes’ que curan las heridas de forma más rápida y segura
- El cuarto paciente que se cura del VIH: logra librarse del sida tras recibir un implante de células madre